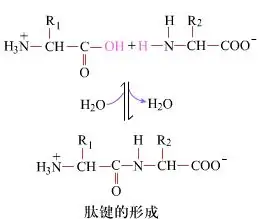
Ing permukaan, pambentukan ikatan peptida, ngasilake dipeptida, minangka proses kimia sing prasaja.Iki tegese loro komponen asam amino disambungake dening ikatan peptida, ikatan amida, nalika dehidrasi.
Pembentukan ikatan peptida yaiku aktivasi asam amino ing kahanan reaksi sing entheng.(A) bagean karboksil, asam amino kapindho (B) Bagian karboksil aktif nukleofilik banjur mbentuk dipeptida (AB)."Yen komponen karboksil (A) ora dilindhungi, pambentukan ikatan peptida ora bisa dikontrol."Produk sampingan kayata peptida linier lan siklik bisa uga dicampur karo senyawa target AB.Mulane, kabeh gugus fungsi sing ora melu ing pembentukan ikatan peptida kudu direksa kanthi cara sing bisa dibatalake kanthi sementara sajrone sintesis peptida.
Dadi, sintesis peptida - pambentukan saben ikatan peptida - kalebu telung langkah agregasi.
Langkah pisanan yaiku nyiyapake sawetara asam amino sing mbutuhake perlindungan, lan struktur zwitterionic asam amino ora ana maneh.
Langkah kapindho yaiku reaksi rong langkah kanggo mbentuk ikatan peptida, ing ngendi gugus karboksil saka asam amino sing dilindhungi N pisanan diaktifake dadi perantara aktif lan banjur ikatan peptida dibentuk.Reaksi gabungan iki bisa kedadeyan minangka reaksi siji-langkah utawa minangka rong reaksi berurutan.
Langkah katelu yaiku mbusak selektif utawa mbusak lengkap saka basa protèktif.Sanajan kabeh penghapusan mung bisa kedadeyan sawise kabeh rantai peptida wis dirakit, mbusak selektif klompok protèktif uga dibutuhake kanggo nerusake sintesis peptida.
Amarga 10 asam amino (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, His, Sec lan Cys) ngemot gugus fungsi rantai samping, sing mbutuhake proteksi selektif, nggawe sintesis peptida luwih rumit.Basis perlindungan sementara lan semi-permanen kudu dibedakake amarga syarat sing beda kanggo selektivitas.Kelompok proteksi sauntara digunakake ing langkah sabanjure kanggo nggambarake proteksi sementara asam amino utawa gugus fungsi karboksil.Klompok protèktif semi-permanen dibusak tanpa ngganggu ikatan peptida sing wis kawangun utawa rantai samping asam amino, kadhangkala nalika sintesis.
"Saenipun, aktivasi komponen karboksil lan pambentukan ikatan peptida (reaksi kopling) kudu cepet, tanpa pembentukan rasemik utawa produk sampingan, lan reaktan molar kudu ditrapake kanggo ngasilake dhuwur."Sayange, ora ana cara kopling kimia sing nyukupi syarat kasebut, lan sawetara sing cocog kanggo sintesis praktis.
Sajrone sintesis peptida, gugus fungsi sing ana ing macem-macem reaksi biasane disambungake menyang pusat manual, glisin minangka siji-sijine pangecualian, lan ana risiko potensial rotasi.
Langkah pungkasan ing siklus sintesis peptida yaiku ngilangi kabeh klompok protèktif.Ngilangi klompok protèktif sing selektif penting kanggo ekstensi rantai peptida saliyane syarat kanggo ngilangi proteksi lengkap ing sintesis dipeptida.Strategi sintetis kudu direncanakake kanthi teliti.Gumantung ing pilihan strategis, N bisa selektif mbusak klompok α-amino utawa carboxyl nglindhungi.Istilah "strategi" nuduhake urutan reaksi kondensasi asam amino individu.Umumé, ana bedane antarane sintesis bertahap lan kondensasi fragmen.Sintesis peptida (uga dikenal minangka "sintesis konvensional") dumadi ing solusi.Umume kasus, dawa bertahap saka ranté peptida mung bisa disintesis kanthi nggunakake ranté peptida kanggo nyintesis fragmen sing luwih cendhek.Kanggo nyintesis peptida sing luwih dawa, molekul target kudu dipérang dadi fragmen sing cocog lan ditemtokake manawa bisa nyuda tingkat diferensiasi ing terminal C.Sawise fragmen individu dirakit kanthi bertahap, senyawa target bakal digabung.Strategi sintesis peptida kalebu pilihan fragmen protèktif sing paling apik lan paling cocok, lan strategi sintesis peptida kalebu pilihan kombinasi basa protèktif sing paling cocok lan cara konjugasi fragmen sing paling apik.
Posting wektu: Jul-19-2023